耐高壓臭氧發(fā)生器用于超濾膜曝氣污水處理應用
一���、研究背景與意義
1. 水傳播病原體危害:水傳播病原體與傳染病相關�����,是公共衛(wèi)生的重大威脅�,全球每年約100萬人因飲用水不安全、環(huán)境衛(wèi)生不足和手部衛(wèi)生差死于腹瀉疾病�����。
2. 傳統(tǒng)消毒方式局限:常用消毒劑如氯����、二氧化氯和臭氧存在問題���,過量使用化學消毒劑會產生有毒消毒副產物�,還會導致微生物耐藥性,對公共衛(wèi)生造成額外風險���。
3. 臭氧消毒的優(yōu)缺點:臭氧因氧化電位高(2.07V)且產物無毒(O?),被美國環(huán)保署推薦為替代傳統(tǒng)氯消毒的消毒劑���,能有效殺滅微生物���,如20ppm臭氧可在4分鐘內滅活空氣中的煙曲霉菌�����,且臭氧化過程中會產生強氧化劑羥基自由基(?OH)輔助消毒�����。但傳統(tǒng)臭氧化在水中的傳質速率有限(約0.04min?1),導致臭氧消耗量大���、能耗高,限制了其廣泛應用�����。
4. 傳統(tǒng)曝氣方式不足:依賴鈦合金曝氣器或沖擊器的傳統(tǒng)臭氧曝氣通常產生毫米氣泡�����,這類氣泡上升速度快����、氣液接觸面積有限�����,傳質效率低��,氧氣轉移效率僅6%-10%��,需更高臭氧劑量才能達到預期效果��,增加能耗并造成環(huán)境負面影響。
5. 微氣泡曝氣的潛力:微氣泡曝氣能提高臭氧轉移速率����,微氣泡直徑1-100μm,可將臭氧利用率提升至65%-79%��。陶瓷超濾膜曝氣能耗低�����、設備簡單��,是極具應用潛力的微氣泡曝氣方法����,但目前關于陶瓷膜微氣泡系統(tǒng)在水中的消毒性能及強化微生物消毒機制的研究有限,故開展本研究�。
二���、研究材料與方法
(一)材料與化學試劑
1. 培養(yǎng)基類:營養(yǎng)肉湯、MS2噬菌體液體培養(yǎng)基���、Luria-Bertani(LB)營養(yǎng)瓊脂�、營養(yǎng)瓊脂和MS2噬菌體半固體培養(yǎng)基。
2. 化學試劑:對氯苯甲酸(pCBA�����,>99.0%���,GC)、2,4-二硝基苯肼(98%��,AR�,用于HPLC)、冰醋酸(99.5%�,AR)和靛藍三磺酸鉀(55%�����,用于HPLC)�����;麥克林生化科技有限公司提供甲酸(99%,用于HPLC)����、十二水合磷酸氫二鈉(99%����,GR)�、磷酸二氫鈉(99.9%)��、硫代硫酸鈉(99%)和磷酸(AR)����;蘇州安特食品有限公司提供無水乙醇�;上海羅恩化學科技有限公司提供乙酸鈉����;上海安譜科學儀器有限公司提供叔丁醇(TBA�����,用于HPLC)和乙腈(HPLC級)�。
3. 實驗用水:采用Milli-Q水系統(tǒng)(美國Millipore)制備去離子水�����,經高壓滅菌器(松下MLS-3751L)滅菌����,除非另有說明����,所有溶液均用滅菌去離子水配制�。
(二)臭氧曝氣實驗系統(tǒng)
1. 臭氧來源:由高壓臭氧發(fā)生器(北京同林代理的加拿大Absolute Ozone ATLAS P30)使用99.999%純氧提供臭氧��。
2. 流量與濃度監(jiān)測:通過質量流量計(北京杰銳TSK621)控制進氣臭氧流量���,利用臭氧在線分析儀(北京同林科技3S-J5000)監(jiān)測進出口氣態(tài)臭氧濃度���。
3. 反應裝置:在有機玻璃制成的反應器(內徑6.8cm、高度30cm����、體積1.2L)內進行曝氣�����,反應器下方設有磁力攪拌器以保證氣泡均勻分布����。
4. 曝氣方式:將平板陶瓷膜(7.4mm×6mm×0.38mm)固定在反應器底部用于微氣泡曝氣�,氣態(tài)臭氧通過陶瓷膜 pores(直徑50nm)產生微氣泡���;采用鈦微孔曝氣器進行毫米氣泡曝氣,通過氣管連接在玻璃反應器底部���。
(三)微生物選擇與制備
1. 選擇的微生物:從中國普通微生物菌種保藏中心(CGMCC)購買4種水中常見細菌,以大腸桿菌(E. coli���;CGMCC 1.3373)和銅綠假單胞菌(P. aeruginosa,CGMCC 1.12483)作為革蘭氏陰性菌代表��,金黃色葡萄球菌(S. aureus��,CGMCC 1.12409)和糞腸球菌(E. faecalis�����,CGMCC 1.2135)作為革蘭氏陽性菌代表;選用MS2噬菌體(ATCC 15597)作為非包膜病毒模型���,其為單鏈RNA病毒,與腸道病毒相似���。
2. 微生物制備:詳細步驟見支持信息(Text S1)。
(四)消毒實驗
1. 實驗設置:模型微生物初始濃度��,細菌為3.8-7.2×10?菌落形成單位/毫升(CFU/mL)���,病毒為3.8-7.2×10?空斑形成單位/毫升(PFU/mL)���。向反應器內1L滅菌磷酸鹽緩沖液(PBS,5mM����,pH 7.16)中加入1mL模型微生物儲備液,進行臭氧曝氣��,臭氧進口濃度設定為10mg/L并實時監(jiān)測,根據(jù)總臭氧劑量(TOD)計算臭氧投加量�。
2. 樣品處理:取樣時用1.5倍化學計量比的硫代硫酸鈉淬滅樣品,收集的樣品用于評估消毒效果�。
3. 實際水樣實驗:將大腸桿菌加入自來水�����、河水和二級出水樣品中���,所有水樣使用前經0.22μm聚醚砜膜過濾去除原有細菌�,4℃儲存�����,然后按上述方法進行消毒實驗����,水樣水質參數(shù)見支持信息(Table S1)�����。
4. 濃度測定:采用標準涂布平板法[20]測定細菌濃度����,雙瓊脂層法[57]測定病毒濃度����,詳細方法見Text S2�;通過總臭氧劑量(TOD�,公式1)衡量氣態(tài)臭氧暴露量�,公式中V為水樣體積(L)�����,t為曝氣時間(min)���,[O?]inlet?和[O?]outlet?分別為進出口氣態(tài)臭氧濃度(mg/L),Q為氣態(tài)臭氧流量(mL/min)[16]�。
(五)分析方法
1. 細胞形態(tài)分析
-細菌形態(tài):采用掃描電子顯微鏡(SEM)[21]評估消毒前后細菌形態(tài)����,8000rpm離心收集細菌樣品�����,加入1.5%戊二醛在4℃下固定過夜��,PBS洗滌三次后�,用不同濃度乙醇溶液(10%、30%�����、50%��、70%����、80%�����、90%或100%)脫水���,再加入叔丁醇(50%����、70%或100%)置換乙醇,冷凍干燥機(日本Eyela FDU-1110)干燥后����,通過SEM(日本Hitachi SU8010)觀察����。
-病毒形態(tài):采用透射電子顯微鏡(TEM)觀察病毒形態(tài),消毒前后樣品中加入2%戊二醛在4℃下固定過夜��,1%磷鎢酸染色后����,將一滴病毒樣品滴在銅網上進行透射電子顯微鏡觀察。
2. 膜損傷流式細胞術分析
-膜完整性:使用細菌活力試劑盒(美國Thermo Fisher Scientific LIVE/DEAD BacLight L7007)表征細菌膜完整性�,該試劑盒含SYTO 9和碘化丙啶(PI)兩種染料���,按1:6摩爾比將SYTO 9和PI混合物加入1mL細菌樣品中��,暗處孵育15min后進行流式細胞術(美國Beckman CytoFLEX)分析[23,22]。
-膜電位:使用雙-(1,3-二丁基巴比妥酸)三甲川氧雜蒽醇(DiBAC4(3)�����,美國Biotium)表征膜電位����,向1mL細菌樣品中加入5μM DiBAC4(3)�����,37℃孵育30min后進行流式細胞術分析���。
3. 細菌代謝活性檢測:采用Alamar Blue試劑(中國Maokang MX3006)分析細菌代謝活性,將細菌樣品與Alamar Blue染料和營養(yǎng)肉湯混合置于黑色96孔板中����,孵育6h后����,通過熒光酶標儀(美國Molecular Devices Spectra Max I3)測定樣品熒光強度,按公式(2)計算細菌代謝活性��,其中F?為陰性對照組平均熒光強度����,F(xiàn)?為陽性對照組平均熒光強度����,F(xiàn)為樣品平均熒光強度�����。
4. DNA損傷分析:采用凝膠電泳進行DNA損傷分析[23,42]����,使用Magen HiPure細菌DNA提取試劑盒(中國Magen D3146-02)提取大腸桿菌DNA�,凝膠成像儀(美國Bio-Rad Gel Doc XR)對含DNA的凝膠成像�����,詳細步驟見Text S3���。
5. 臭氧曝氣分析:激光粒度分析儀(英國Malvern Mastersizer 3000)測定曝氣臭氧氣泡的直徑分布��;靛藍三磺酸鉀法[3]測定水中臭氧濃度�;通過叔丁醇(TBA)與?OH的反應(Text S4)[49]確定?OH產率�����;采用高效液相色譜(日本Shimadzu LC-2030)按先前研究[16]描述的方法檢測對氯苯甲酸(pCBA)濃度。
6. 臭氧傳質模擬:采用有限元法和ANSYS Fluent軟件模擬臭氧分布,針對單個微氣泡和毫米氣泡分析�����,根據(jù)氣泡實際尺寸建立二維模型��;曝氣過程中建立反應器二維軸對稱模型�����,利用Fluent計算流體動力學模擬微氣泡和毫米氣泡曝氣�����,依據(jù)薄材料傳遞模擬臭氧傳質����,模擬過程中使用的參數(shù)(Table S2)反映實際曝氣條件��。
7. 能耗計算:能耗是評估成本和環(huán)境影響的重要指標�����,本研究中大部分能耗為臭氧產生所需電能[28,48]��,通過公式(3)計算單位階躍電能(EEO)�,其中P??為產生1g臭氧所需電能(10Wh/g-O?)��,TOD為消毒所需總臭氧劑量(mg/L)�����,V為微生物懸浮液體積(L)��。
8. 統(tǒng)計分析:使用Origin軟件進行Tukey事后檢驗分析顯著差異���,概率小于一定值時認為具有統(tǒng)計學意義���。
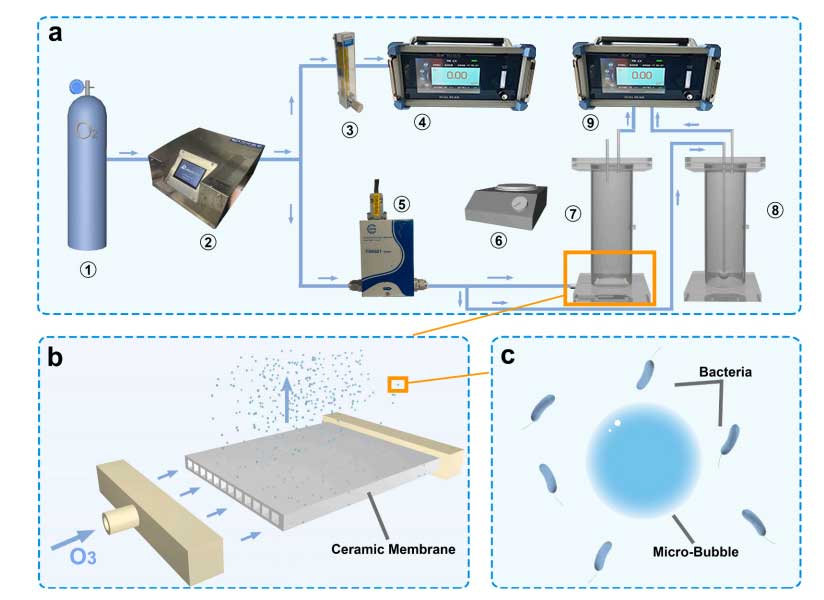
臭氧曝氣系統(tǒng)���。(a)臭氧曝氣系統(tǒng)的氣路。1)氧氣瓶�����;2)臭氧發(fā)生器��;3)流量計;4)臭氧氣體濃度檢測器����;5)質量流量計��;6)磁力攪拌器;7)微泡曝氣塔�;8)微泡曝氣塔;9)出口臭氧氣體濃度檢測儀�����。(b)陶瓷膜曝氣示意圖�。(c)微泡與細菌示意圖���。
三�����、研究結果與討論
(一)臭氧曝氣消毒性能
1. 不同曝氣方式對比:對比臭氧微氣泡曝氣與毫米氣泡曝氣對五種代表性微生物(兩種革蘭氏陰性菌:大腸桿菌和銅綠假單胞菌;兩種革蘭氏陽性菌:金黃色葡萄球菌和糞腸球菌���;一種模型病毒:MS2噬菌體)的消毒性能����,總體而言���,達到五種微生物4個數(shù)量級(99.99%)滅活效果��,毫米氣泡曝氣所需臭氧劑量是微氣泡曝氣的三倍以上(圖2a-2e和Table S3)�。
2. 對不同細菌的消毒效果
-革蘭氏陰性菌:微氣泡曝氣在極低總臭氧劑量(0.026mg/L)下對大腸桿菌實現(xiàn)3.2個數(shù)量級滅活�,而該劑量下毫米氣泡曝氣無明顯消毒效果�����;總臭氧劑量分別增至0.15mg/L和0.75mg/L時,大腸桿菌和銅綠假單胞菌實現(xiàn)完全滅活(>6個數(shù)量級)����。
-革蘭氏陽性菌:革蘭氏陽性菌對臭氧抗性更強,總臭氧劑量增至0.05mg/L時����,微氣泡曝氣對金黃色葡萄球菌的滅活率快速達到3.1個數(shù)量級��,總臭氧劑量1.78mg/L時��,滅活率進一步提升至6.4個數(shù)量級;而毫米氣泡曝氣在該總臭氧劑量下僅實現(xiàn)約3個數(shù)量級滅活��。
3. 細菌抗性差異原因:革蘭氏陰性菌更易被滅活��,這與其細胞膜組成有關����,革蘭氏陰性菌外膜成分是脂蛋白和脂多糖[40]���,易被臭氧氧化;而革蘭氏陽性菌細胞上有更厚的肽聚糖層���,對臭氧抗性更強[62]����?���?傮w而言��,相同總臭氧劑量下�,微氣泡曝氣比毫米氣泡曝氣提高了臭氧消毒效率��。
4. 實際水樣消毒效果:評估臭氧微氣泡曝氣在實際水樣(自來水�、湖水和二級出水)中的消毒性能(圖2f)�����,所有情況下���,總臭氧劑量1.0mg/L內均實現(xiàn)大腸桿菌4個數(shù)量級(99.99%)滅活���;自來水和河水中,總臭氧劑量分別為0.38mg/L和0.72mg/L時��,大腸桿菌實現(xiàn)完全滅活�����,表明臭氧微氣泡曝氣在不同實際水樣中均具有有效的消毒效果��。
(二)消毒性能增強機制
1. 微氣泡物理特性與消毒貢獻:陶瓷膜產生的臭氧微氣泡直徑范圍為9.25-92.05μm(圖3a),微氣泡中位直徑(25.5±1.3μm)僅為毫米氣泡(1646.7±270.6μm)的1.5%(Figure S2)���。已有研究表明微氣泡與毫米氣泡物理特性不同,微氣泡的破裂和收縮可產生強烈的機械剪切應力和壓力波�����,并產生自由基[24]���,可能有助于消毒。通過氧氣微氣泡曝氣研究物理力對消毒的貢獻(圖3b-3c)�����,與臭氧微氣泡曝氣相比�����,氧氣微氣泡曝氣對大腸桿菌或金黃色葡萄球菌無明顯消毒效果���,表明本系統(tǒng)中微氣泡物理力的貢獻可忽略不計�����;而臭氧微氣泡曝氣對大腸桿菌和金黃色葡萄球菌分別實現(xiàn)6.3個數(shù)量級和4.5個數(shù)量級滅活��,說明臭氧化的化學氧化作用在微生物消毒中起主導作用。
2. 臭氧傳質與?OH生成:臭氧微氣泡曝氣促進臭氧傳質和?OH生成����,由于微氣泡曝氣高效的臭氧氣液傳質,其平衡水中臭氧濃度是毫米氣泡曝氣的2.38倍(圖3d)���,這歸因于臭氧表觀傳遞速率,是毫米氣泡曝氣的2.80倍(Figure S3)��。溶解臭氧越多�,?OH暴露量越大,微氣泡曝氣的累積?OH是毫米氣泡曝氣的3.68倍(圖3e)�����,具體而言�,微氣泡曝氣的?OH產率比毫米氣泡曝氣提高2.40倍(Figure S4)����,從而產生更多?OH����。以pCBA為探針評估?OH穩(wěn)態(tài)濃度(圖3f)�����,微氣泡曝氣下pCBA降解更快�����,進一步證明臭氧微氣泡曝氣導致更高的?OH暴露量�。
3. 臭氧與?OH的消毒貢獻:為探究臭氧直接消毒和?OH間接消毒的貢獻��,對比有無叔丁醇(TBA)時臭氧微氣泡曝氣的消毒性能��,TBA常被用于猝滅?OH,且對細菌無明顯殺滅作用[49]����。添加TBA導致大腸桿菌和金黃色葡萄球菌的滅活速率常數(shù)均略有下降(圖3g),表明臭氧氧化和?OH氧化均有助于消毒�����,且臭氧分子的直接氧化是微生物滅活的主要原因。
4. 臭氧傳質有限元模擬:采用有限元模擬進一步分析微氣泡曝氣的臭氧傳質�,構建單個氣泡模型以了解氣泡尺寸對臭氧傳質的影響,直徑25.5μm的微氣泡比毫米氣泡具有更強的傳質能力�,1秒內氣泡中95.82%的臭氧從氣相轉移到液相(不考慮氣泡的收縮和破裂)(圖3h)�����;而直徑1.65mm的毫米氣泡中僅1.27%的臭氧從氣相轉移到液相��。相同流量下���,微氣泡曝氣產生更多氣泡��,傳質熱點大幅增加�����,因此微氣泡曝氣導致更高的臭氧暴露和?OH暴露���。反應器內曝氣模擬結果顯示�����,5秒內微氣泡曝氣的平均臭氧濃度達到0.82mg/L�,而毫米氣泡曝氣僅為0.041mg/L(圖3i)�����,臭氧微氣泡曝氣在整個反應器內產生更高的臭氧暴露(Figure S5)�,對微生物造成更大損害,提高消毒性能��。
5. 能耗對比:計算兩種臭氧曝氣系統(tǒng)的EEO值��,對于所有微生物����,臭氧微氣泡曝氣的EEO值均低于毫米氣泡曝氣(圖3j)��,表明臭氧微氣泡曝氣是一種高效且經濟的微生物完全滅活方法。
(三)臭氧誘導微生物損傷表征
1. 微生物形態(tài)變化:通過掃描電子顯微鏡(SEM)和透射電子顯微鏡(TEM)觀察微生物形態(tài)變化以研究臭氧曝氣后的細胞結構損傷(圖4a)����?���;畹拇竽c桿菌表面光滑��、結構完整[38,47];毫米氣泡曝氣后���,大腸桿菌表面略有收縮����,但結構仍相對完整,表明損傷較?����?��;而微氣泡曝氣后,大腸桿菌表面塌陷且出現(xiàn)孔洞���。革蘭氏陽性菌(金黃色葡萄球菌)經臭氧微氣泡曝氣后發(fā)生收縮����,而臭氧毫米氣泡曝氣后未觀察到明顯的結構變化(圖4b),表明細胞壁更厚的革蘭氏陽性菌對臭氧損傷的抗性更強���。MS2噬菌體經臭氧微氣泡曝氣后,衣殼明顯扭曲和斷裂(圖4c)��,說明與毫米氣泡曝氣相比���,微氣泡曝氣對細菌細胞和病毒衣殼結構造成更嚴重的破壞���。
2. 大腸桿菌膜完整性與膜電位:采用流式細胞術進一步評估大腸桿菌細胞膜完整性(圖4d)�,SYTO 9可穿透所有細菌的膜并與細胞核結合標記所有細菌���,PI僅能穿透受損細菌�,可用于標記細胞膜受損的細菌并評估膜損傷程度[52]�����。根據(jù)PI和SYTO 9信號強度,流式熒光點圖分為四個象限(Q1-Q4)�,Q1為SYTO 9信號高、PI信號弱的完整細胞�,Q2為SYTO 9和PI信號均高的輕度受損細胞,Q3為PI信號高���、SYTO 9信號低的嚴重受損細胞,Q4為未明顯染色的細胞碎片[31]�����。處理前���,91.94%的細菌處于Q1;微氣泡曝氣后�����,98.51%的細菌處于Q3����,表明該處理造成嚴重的細胞損傷�;毫米氣泡曝氣后�����,43.56%的細菌處于Q2��,51.34%的細菌處于Q3��,表明毫米氣泡曝氣造成的損傷較小���,這與SEM表征結果一致。細胞膜電位變化也與此相符(圖4e)����。
3. 大腸桿菌代謝活性:采用Alamar Blue(一種無毒且可穿透細胞的染料)評估大腸桿菌的代謝活性(圖4f)����,該藍色染料可被細胞攝取并在細胞內還原為粉紅色的試鹵靈,通過測量熒光可確定細菌的代謝活性���。毫米氣泡曝氣后細菌的代謝活性高達處理前的90%�;而微氣泡處理后,細菌的代謝活性僅為處理前的3.19%����。結果表明��,微氣泡曝氣提高了臭氧濃度,造成嚴重的細胞膜損傷����,使臭氧能夠進入細胞并氧化細胞內成分,從而破壞細胞代謝活性��,臭氧微氣泡曝氣極大地損害了細胞活力并誘導細胞死亡[59]�����。
4. 大腸桿菌DNA損傷:通過凝膠電泳評估DNA完整性���,證實臭氧微氣泡曝氣對細胞內成分的損傷[25]��?����;罴毦腄NA條帶亮度集中在42.5kb處(圖4g);微氣泡曝氣0.5min后,核酸條帶分散���,曝氣1.5min后無明顯條帶,表明持續(xù)的臭氧氧化使DNA完全破壞或斷裂成小片段���。細胞膜受損時,臭氧可能進入細菌并氧化細胞內物質和DNA�����。對于毫米氣泡曝氣�����,處理1min時仍可觀察到核酸條帶�����,之后隨著曝氣時間增加才逐漸分散,表明即使在低總臭氧劑量下�,微氣泡曝氣對DNA的損傷也比毫米氣泡曝氣更大。
(四)微氣泡曝氣增強臭氧消毒機制
根據(jù)實驗結果得出的消毒機制如圖5所示�,微氣泡曝氣顯著提高了臭氧的傳質速率���,使水中的平衡臭氧濃度更高(圖3d)��。此外�,在相同流速下��,與毫米氣泡曝氣相比,微氣泡曝氣產生更多的氣泡���,增加了臭氧與微生物的接觸面積[61]��。因此����,微生物暴露在更高濃度的臭氧中,導致更嚴重的膜損傷(圖5a)��,這種損傷是由于臭氧與細菌接觸后迅速降解細胞膜表面成分[10]�����,導致細胞內容物泄漏和細菌收縮(圖4a-4b)����。此外���,臭氧通過受損的細胞膜迅速進入細胞,氧化并破壞DNA等細胞內成分(圖4g)����,導致細胞活力大幅下降(圖5b)?����?傮w而言,微氣泡曝氣是一種增強臭氧對微生物消毒效果的有效方法���,與毫米氣泡曝氣相比���,微氣泡曝氣實現(xiàn)微生物完全滅活所需的臭氧劑量更低��。
四、研究結論
1. 消毒效果顯著:低總臭氧劑量(約1.0mg/L)即可有效實現(xiàn)完全消毒��,降低了大腸桿菌和MS2噬菌體6個數(shù)量級滅活所需的總臭氧劑量��,同時將金黃色葡萄球菌和糞腸球菌的消毒效果提升了3個數(shù)量級。
2. 傳質與?OH生成優(yōu)勢:優(yōu)異的消毒性能源于臭氧傳質能力的增強和?OH生成的增加�����,與毫米氣泡曝氣相比��,微氣泡曝氣有效提高了平衡水中臭氧濃度(1.38倍)和?OH產率(2.40倍)��。
3. 微生物損傷嚴重:細菌膜的成分和結構受到嚴重破壞,細胞內細菌DNA被氧化和斷裂�,導致細胞活力大幅下降(>80%),降低了基因釋放到水中的風險����。
4. 實際應用潛力與挑戰(zhàn):本研究中使用的耐腐蝕陶瓷膜延長了微氣泡曝氣在實際應用中的使用壽命���,但實際水體成分復雜(含膠體��、顆粒、溶解性有機物和離子)��,可能導致膜污染或堵塞�����?���?赏ㄟ^預處理�����、工藝參數(shù)優(yōu)化和定期清洗等策略延長膜的使用壽命�����,未來需進一步研究不同水質條件下微氣泡曝氣的長期性能。
5. 綜合效益良好:微氣泡曝氣對多種病原微生物(包括各種革蘭氏陰性菌��、革蘭氏陽性菌以及病毒)表現(xiàn)出優(yōu)異的消毒性能���,且對不同微生物的能耗降低了37.2%以上���。通過降低所需氧化劑劑量�����,臭氧微氣泡曝氣為更可持續(xù)�、更安全的水處理做出了貢獻。
五���、環(huán)境意義
臭氧實際應用中存在傳質速率低的問題�,需高臭氧劑量和高能耗才能達到消毒目標。本研究提出的微氣泡曝氣方法克服了傳統(tǒng)曝氣的局限性�����,能以低臭氧需求量實現(xiàn)對多種微生物的綠色高效消毒�����,微生物滅活能耗降低37.2%�����,研究結果凸顯了微氣泡曝氣在降低臭氧消毒總成本和環(huán)境影響方面的潛力����。
六�����、附錄說明
與本文相關的補充數(shù)據(jù)可在在線版本(doi:10.1016/j.jhazmat.2025.138174)中找到���。



 當前位置:
當前位置: 
 摘要
摘要 上一篇:
上一篇: 返回列表
返回列表
